该病例讨论由南非开普敦Tygerberg学术医院Charles KYRIAKAKIS医生和Hellmuth WEICH医生提供给PCRonline网站。
病例汇报
1例16岁男性因胸骨下压榨性疼痛伴放射至左臂6小时就诊于南非开普敦Tygerberg学术医院的胸痛中心。入院时患者无胸痛,血液动力学稳定,心率80次/分,血压130/80 mm Hg,无心力衰竭。否认违禁药物服用史,心血管危险因素有腰围增加、吸烟、低密度脂蛋白胆固醇(LDL-C)6.0 mmol/L,脂蛋白Lp(a)3.27 g/L(<0.03 g/L)。12导联心电图示窦性心律,等律性房室分离,动态下侧壁T波倒置(图1)。床旁经胸超声心动图(TTE)显示左室无扩张,射血分数50%,中下壁运动减弱,瓣膜功能正常,未见新生物或血栓。
.jpg)
图1 入院时12导联心电图
入院后,患者开始双联抗血小板药物、低分子量肝素、高剂量他汀和β受体阻滞剂治疗。初始高敏心肌肌钙蛋白(hs-cTnI)1792 ng/L [世界卫生组织急性冠状动脉综合征(ACS)诊断阈值是600 ng/L],次日早晨复查值> 50 000 ng/L。
尽管患者年仅16岁,非ST段抬高型心肌梗死(NSTEMI)的诊断成立,根据心电图和TTE结果,考虑右冠状动脉(RCA)最可能为罪犯血管。由于患者hs-cTnI值极高伴下侧壁T波倒置,还考虑自发性再灌注的下侧壁ST段抬高型心肌梗死(STEMI)可能性。
入院后次日患者接受冠状动脉造影,右侧桡动脉入路。心室造影证实中下壁运动减弱;RCA未见阻塞(图2);左冠状动脉(LCA)第一次注射造影剂时即可见左主干体部高度活动的充盈缺损,左前降支(LAD)和左回旋支(LCX)未见阻塞(图3)。
.jpg)
图2 RCA未见阻塞
.jpg)
图3左主干体部充盈缺损
尽管心电图、TTE和心室造影均指向RCA是罪犯血管,但血管造影发现RCA未见阻塞。左主干体部高度活动的充盈缺损的病因可能有:
-
导管血栓被注入LCA;
-
自发性或医源性冠状动脉夹层;
-
来自心脏血栓或赘生物的血栓栓塞;
-
相对健康血管的原发性血栓形成;
-
来自心脏新生物的栓塞,如瓣膜乳头状弹力纤维瘤。
病例讨论
临床工作中罕见十几岁少年以ACS就诊。ACS年轻患者最常见的病因是违禁药物服用史,以甲基苯丙胺最为普遍,诱发冠状动脉痉挛,导致冠状动脉内淤滞和血栓形成。此例患者无违禁药物服用史,我们不得不考虑可以解释左主干充盈缺损的各种原因。
由于高度怀疑RCA为罪犯血管,所以发现左主干充盈缺损而RCA正常时很惊异。在造影时,6-F JL 3.5诊断导管非常小心地进入左主干,因此导管导致的医源性夹层可能性很小。而且充盈缺损在第一次注入造影剂即可见,不是出现于左主干开口处,而是位于体部,更进一步排除医源性夹层可能性。
我们的导管室操作流程要求桡动脉入路时,当JL诊断导管通过主动脉弓后,立即静脉注射5000 iu肝素。该患者在造影的早晨未皮下注射低分子量肝素,在造影过程中给予静脉肝素。充盈缺损位于左主干内,并没有栓塞远端LCA。鉴于以上原因,导管血栓也基本可排除。
其他可能病因还有:自发性冠状动脉夹层血栓;无血流限制性斑块破裂血栓;来自心脏的血栓或新生物导致的栓塞。为进一步了解左主干情况,行血管内超声(IVUS),发现左主干体部有一个带蒂的高度活动的团块。IVUS虚拟组织学证实其为含坏死核心的斑块,体积小,非薄帽,斑块大部分由纤维组织组成,散在小的纤维脂肪组织(图4)。Chromoflow未能识别可能的夹层撕裂皮瓣。
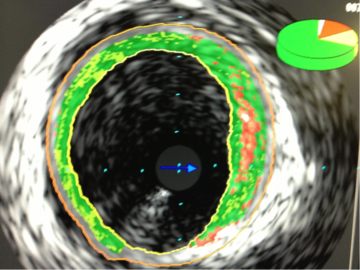
图4 IVUS虚拟组织学显示的斑块
我们一致认为常规ACS支架置入不适用于该例患者。血栓抽吸不仅可以避免远端冠状动脉栓塞,还可对抽吸组织进行组织学检测。抽吸出的团块很坚硬,呈红-白色(图5)。组织学检测证实其为纤维蛋白血栓,因此该患者病因为新生冠状动脉内血栓形成,考虑患者可能存在高凝状态。未能探查到患者有血栓形成倾向的原因。出院时继续予双联抗血小板治疗和高剂量他汀,无症状。
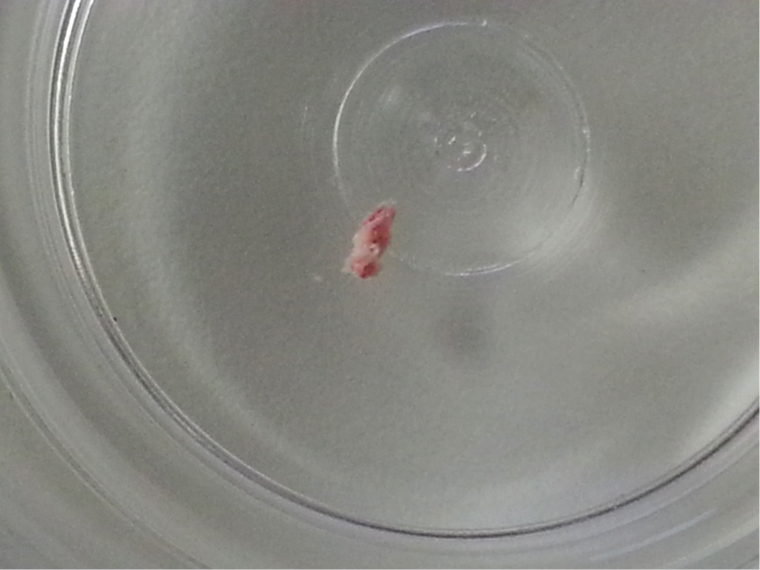
图5 抽吸出的纤维蛋白血栓
6个月后患者以肾病综合征就诊,肾脏活检证实局灶性节段性肾小球硬化(FSGS)。排除继发FSGS的病因后,确认其病因为肥胖引起的肾小球超滤。回顾患者6个月前ACS入院时的病史记录,发现入院时蛋白尿3+,但接诊医生未汇报。肾脏科医生会诊后,认为当时患者为亚临床肾病综合征,处于高凝状态,导致左主干新生血栓形成,发生ACS。