 姚建民 北京军区总医院
姚建民 北京军区总医院
随着人们生活方式的改变和社会的老龄化,主动脉瓣硬化、钙化与狭窄的发病率日益增高。年龄大于65岁的人群中,1/4存在主动脉瓣硬化,而约1/6的主动脉瓣硬化将发展成为主动脉瓣狭窄(aortic stenosis, AS),且一半的轻、中度AS患者将会发展为具有血流动力学异常的SAS。有症状的AS患者预后比较差,易于发生意外心脏事件,AVR是公认的最有效治疗方式;但是,1/3以上的SAS患者左室随后负荷增加而产生相应程度的重构和代偿性肥厚,因而不出现临床症状。对于无症状SAS患者进行AVR的适应症及手术时机争议还比较大。
目前美国心脏协会(AHA)/美国心脏病学学会(ACC)心脏瓣膜病管理指南对SAS的定义为主动脉瓣口面积≤1.0cm2(或0.6 cm2/ m2)或主动脉瓣口峰值流速≥4.0m/s,或平均跨瓣压差≥40mm Hg。
一般来说,主动脉瓣口血流速度测定的重复性最好,而主动脉瓣瓣口面积(AVA)和跨瓣压力阶差容易出现误差。超声的非侵入性跨瓣压力阶差测定与侵入性检查结果具有良好的相关性,因此较少使用心导管检查诊断AS。如果患者多普勒超声所测跨瓣压力阶差与临床体检结果不一致,又需要性行冠状动脉造影者可以行侵入性血流动力学检查。
三维超声、心脏CT和心脏核磁]可以作为AVA测定和确定AS严重程度的辅助检查方法,但这些影像学检查方式主要为主动脉瓣瓣口面积的解剖学分析而不是功能性分析,因此,我们通常低估AS的严重程度。
正方观点:SAS应在出现症状前行AVR
症状SAS在随访的间隔期可能出现患者并未意识到的症状或猝死
SAS合并有典型症状如心绞痛、晕厥或心力衰竭症状(主要是劳力性呼吸困难),唯一有效的治疗方法是AVR,以防止猝死。此外,AVR可以减轻患者的症状,最大限度的提高患者的生活质量。如果未及时行AVR,每月的自然死亡率为2%,3年死亡率高达75%(图1)。
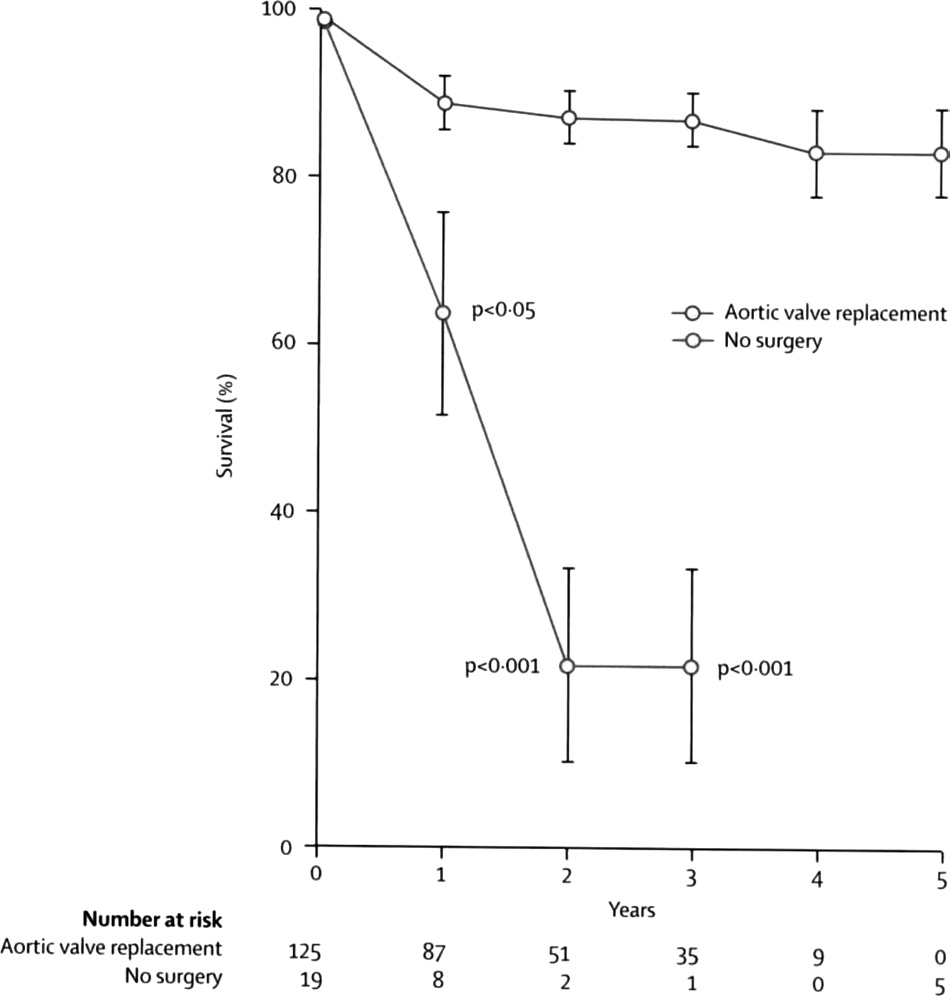
图1. 手术与非手术治疗的疗效对比
无症状SAS患者即使每6个月随访一次,在随访间隔这段时间也可能正好是出现症状或猝死的窗口期。尽管比较好的解决方案是提醒患者,一旦他们出现典型症状必须及时告诉他们的主管医生,但是,这一策略是否有效尚不清楚;并且患者往往很可能根本就难以意识到自己的症状甚或否定这些症状。因此,由于他们不了解等待过程中临床病情的变化,而面临死亡的巨大风险。
无症状SAS在等待期间可能因日常运动而猝死
运动试验是一项评估AS安全有效的辅助手段,三分之一到半数无症状SAS患者的运动试验阳性,其表现为运动耐力下降,运动实验中出现症状或血压未升高到预期值,阳性患者往往在一年内出现症状而需要AVR,未手术者2年生存率不到20%(图2)。因此,无症状SAS应尽早AVR,而不宜等到出现症状才考虑AVR,以免在日常运动中发生猝死风险。
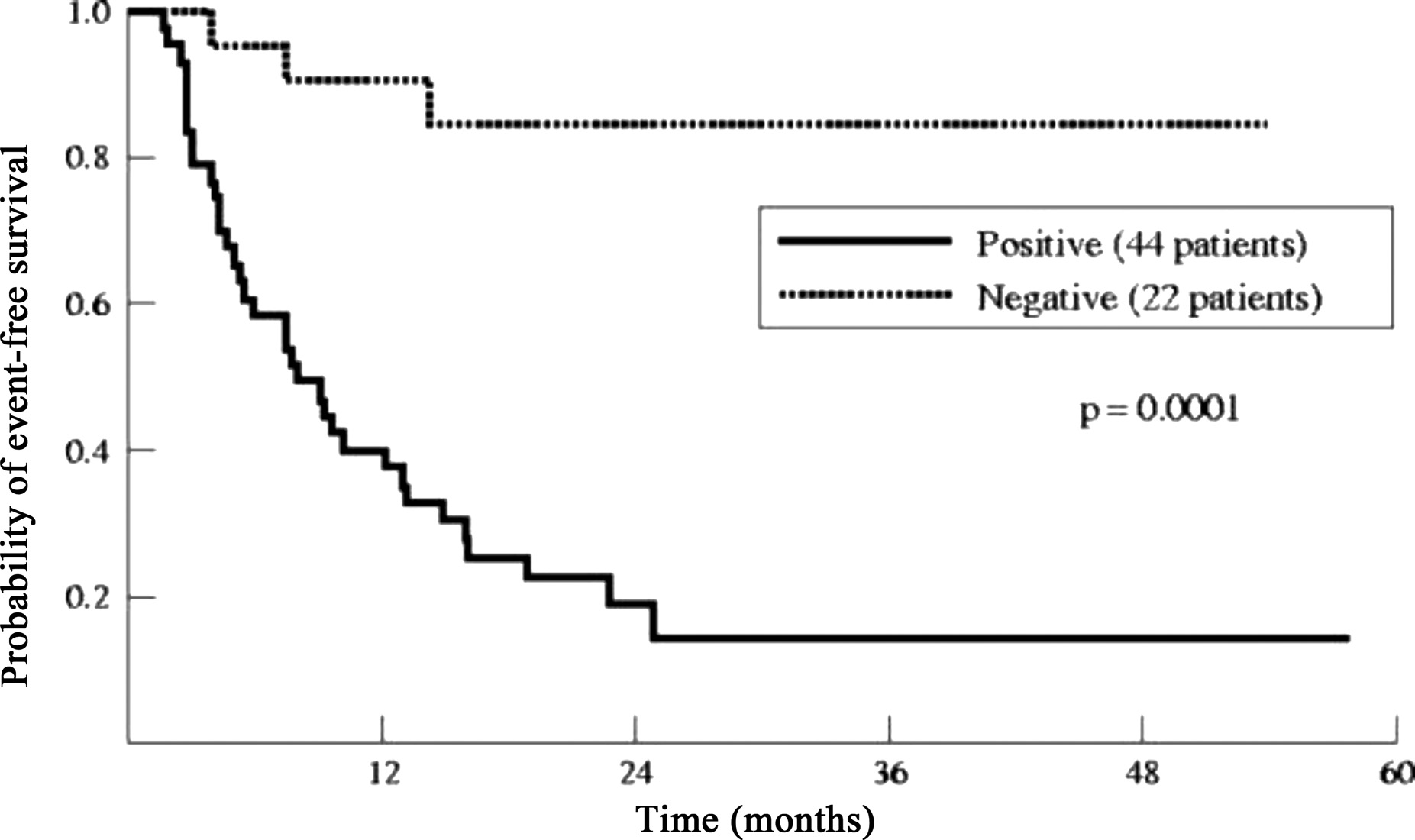
图2. 运动试验患者的生存率情况
无症状SAS在等待期间瓣口狭窄加重、年龄增加,使手术风险增加
AS患者主动脉瓣口面积平均每年减少大约0.1cm2,跨瓣压平均每年大约增加7mm Hg。但是,在一些患者中跨瓣压一年内可增加多达20 mm Hg。主动脉瓣钙化和狭窄越严重,狭窄发展和症状进展越快,如果患者主动脉峰值流速4m/s,绝大部分需要在2两年内行AVR,如果峰值流速>5m/s则需在1年内进行手术。假如不及时手术,在等待出现症状期间,患者的年龄无疑会随之增加,手术风险必将相应增加。根据美国胸外科医师协会对心脏手术风险的评估标准,即使患者在这2年内没有出现其它合并症,如果年龄从73岁增大到75岁,绝对手术死亡风险率增加0.1%,总死亡率和严重并发症发生率增加0.5%。很显然,假设等待期间出现其它严重的健康问题,手术的风险会更高。因此,毋庸置疑在症状出现前的现在手术比2年后手术更安全可行,而等待除了会出现症状外,却不会使患者有任何获益。
由于AS与动脉粥样硬化在病因和病理机制上有许多相似之处,他汀类药物可以有效治疗冠状动脉粥样硬化性心脏病,有学者曾将他汀类药物用于AS的治疗。不幸的是,几项随机试验发现他汀类药物并未能防止不同程度AS的病情进展或延缓症状的发生,因此,不能用他汀类药物治疗而将AVR推迟到出现症状。
无症状SAS在等待期间左心室肥厚加重,使手术风险增加
AS引起的压力负荷过重会导致左心室向心性肥厚,增厚的左心室壁能增加左室收缩力而有利于左室克服前向阻力排出血液,维持正常的血流动力学。但是,AS或其它心脏疾病合并左室肥厚会增加死亡率和心力衰竭的发生率,尤其是当合并有冠心病时更易发生。最近的一项近2000例AS患者行AVR的配对研究表明,合并严重向心性左室肥厚患者的死亡率和并发症发生率为无严重左室肥厚患者的两倍。因此,无症状SAS在等待手术的过程中左室肥厚加重使手术风险增加,尽早手术效果会更好。
患者的年龄和生活方式
80岁人群的自然死亡率要显著高于50岁者, 50岁人的猝死为家庭和社会带来的悲伤显然要远大于高龄者。因此,无症状SAS是否行AVR要考虑年龄因素和患者期望的生活方式。年轻和喜欢室外运动的SAS,宜在出现症状前尽早AVR。
当然,我们必须慎重权衡早期AVR的利弊,AVR的风险取决于患者的危险因素和术者的外科技术与经验,美国胸外科医师协会的统计显示,未合并冠心病及其他全身疾病的70岁老年男性SAS患者,AVR手术的死亡率为0.8%,死亡和严重并发症的总发生率为8.2%。因此,AVR是非常安全的,手术风险甚至低于无症状SAS患者的猝死风险。
反方观点:SAS不应在出现症状前行AVR
无症状SAS的手术风险超过不手术的风险
研究表明大多数SAS可以多年无症状(图3),每年猝死的发病率为0%~4.1%每年,平均约为1%。而<70岁患者的AVR总体死亡率约为1%~3%,如果合并需要处理的冠心病则死亡率达到5%~7%,除了死亡,AVR后脑卒中的发生率为1.4%~4.8%。除了手术死亡率,AVR无论是用生物瓣或机械瓣,都会伴随相关的额外风险,如瓣膜的退行性变/功能衰竭、感染性心内膜炎的危险性增加和抗血栓治疗的相关并发症。因此,对SAS在症状出现前行预防性手术的风险高于不手术、病程自然发展的风险。对于绝大多数真正的无症状的SAS患者来说,随访观察并定期评估病情似乎是更合理的选择。

图3. SAS患者的病程情况
无症状SAS平板运动试验阳性是否应该早期手术尚缺乏大组病例随机临床实验支持
过去认为,无症状SAS是运动实验的禁忌症,主要是担心运动试验可能引起严重并发症。研究表明,经过改良的Bruce方案可以安全的应用于无症状SAS患者,并进行了一些小型临床试验。无症状SAS运动试验的阳性率约30%,表现为出现症状、心肌缺血、严重室性心律失常或运动后血压上升达不到预计值。一般认为无症状SAS运动试验阳性者的合理治疗方法是AVR,由于这些数据来源于观察性研究而非大组病例的随机临床实验,在美国心脏学会/美国心脏病协会和欧洲心脏病学会的指南中,只是将无症状SAS运动试验阳性者作为AVR的IIB类适应症。
无症状SAS的高危人群是否应该早期手术尚缺乏大组病例的随机临床实验支持
无症状SAS出现下列情况属于高危患者:(1)瓣口面积<0.6cm/m2的SAS;(2)主动脉口峰值流速>4.5~5m/s;(3)跨瓣压差和瓣口流速快速增加(每年>0.3m/s);(4)广泛瓣膜钙化;(5)左心室质量异常增加;(6)左室射血分数降低,<50%。瓣口峰值流速超过5m/s尤其是超过5.5m/s的无症状SAS(无论瓣口面积多大),无心脏事件生存率特别差,1年生存率为49%~81%,2年生存率为32%~48%,3年生存率为15%~37%,4年生存率为7%~21%。
Kang等对197例无症状SAS患者进行了手术和非手术的非随机性研究,患者左室射血分数均正常,主动脉瓣口面积<0.75cm2,主动脉瓣口峰值流速>4.5m/s,其中手术102例、非手术95例,平均随访约50个月。手术组患者无1例手术死亡和心源性死亡,仅有3人死于非心脏性疾病;而非手术的常规治疗组18人心源性死亡、10人死于非心脏性疾病。手术组6年的心源性死亡率和总死亡率分别为0%和2%,而非手术的常规治疗组6年的心源性死亡率和总死亡率分别为24%和32%(p<0.001)。因此,有学者主张对存在1个或1个以上高危因素的SAS建议在出现症状前行预防性手术。然而,这种主张尚缺乏足够的证据,试验对象偏少,尽管进行了配对,但仍存在较高的选择偏差性,并且未手术组可能包括了一些当症状出现时拒绝手术的患者,而使未手术组的死亡率增高。因此,SAS是否应该在出现症状前预防性手术治疗仍需进一步评估,最好采用随机试验解决这一一直困扰医生的临床难题。
手术使无症状SAS的医疗费用增加
最近,Gada等人通过模型分析得出一个结论,主动脉瓣置换不仅增加死亡率和非致死不良事件,并且还会增加医疗费用。对于绝大多数无症状SAS患者来说最佳治疗策略是随访观察,只有预期猝死率达到13%或更高者,在症状出现前行预防性手术才是比较好的选择。
本刊评论:无症状性SAS患者需要更加严格的管理
对于SAS患者的管理和治疗是具有挑战性的课题,当前的各种指南推荐基本上是采取随访观察(wait-and-see)策略,即延迟手术直至出现症状,或者是满足出现重度左心室肥厚、运动试验异常等条件时方考虑AVR。一直以来,对这一策略的合理性存在着较大质疑。
AS的病理生理特征、诊断与分级
主动脉瓣的硬化与钙化往往从主动脉瓣的窦部开始,由于血流剪切力的作用使内膜损伤,随后出现炎症细胞浸润、脂质和钙质沉积和成骨样细胞的活化。随着病情发展,钙化部位通常会延伸到瓣叶尖端,从而使主动脉瓣瓣叶增厚、僵硬和运动受限。从主动脉硬化发展至中、SAS的平均时间间隔分别为6年和8年。左心室随着后负荷的日益增加而发生重构和肥厚。室壁厚度增加、容积/质量比率减小和心腔顺应性降低,引起左室舒张功能不全和左室舒张末压升高。肥厚使左室每克心肌的冠状动脉血流减少,即使没有冠状动脉疾病,也表现为冠状动脉血管扩张储备能力降低,出现冠状动脉血流分布不良、心内膜下缺血和心绞痛,而肥厚本身又使心肌对缺血损伤的敏感性增加,一旦发生梗塞,面积更大,死亡率更高。
临床结局的预测因子
年龄≤50岁的无症状SAS患者无AVR、心源性死亡和非心源性死亡事件的生存率显著高于年龄更大的患者。根据超声心动图主动脉瓣口血流速度和主动脉瓣瓣口面积随时间变化的速率可预测临床转归,与主动脉瓣口峰值血流速度低于4.5 m/s的患者相比,≥4.5 m/s的无症状SAS患者心脏事件(AVR、心源性死亡)的相对风险度升高;左室射血分数降低的无症状SAS患者,需要AVR和发生AS相关性心源性死亡事件的相对危险度增高;主动脉瓣瓣口面积每减少0.2 cm2,需要AVR和心源性死亡事件的相对危险度增加;无或仅有轻度主动脉瓣钙化的患者无AVR、心源性死亡和非心源性死亡等事件的生存率明显高于有中度或重度主动脉瓣钙化的患者;搏出功损耗、平均跨瓣压力阶差与左心室压力之比是无症状SAS患者发生AVR和心源性死亡等心脏事件的预测因子,搏出功损耗>26%的患者在随后的3个月中,发生心源性死亡或接受AVR的概率>30% 。
运动试验阴性患者预后较佳,可能不需要AVR治疗。定量运动多普勒超声能够为无症状SAS患者的预后提供有用的信息,从静息到运动峰值,平均主动脉跨瓣压力阶差升高18 mm Hg和AVA<0.752,是发生心脏事件(心绞痛、呼吸困难、晕厥、需住院治疗的心力衰竭、心源性死亡、AVR)的独立预测因子。电子束CT 显示的主动脉瓣钙化可预测患者无重大事件的生存率,主动脉瓣钙化还是无或仅有轻微症状患者无重大事件生存率的独立预测因子。与主观的超声心动图分级相比,电子束CT的优势是能够进行客观的钙化程度定量分析。
指南导向与症状驱使下的手术治疗
ESC指南建议对于无症状SAS的适宜AVR时机为:运动试验阳性、主动脉瓣口血流峰速每年增加>0.3 m/s或显著左心室肥厚。ACC/AHA指南推荐对于无症状SAS患者如伴有运动试验阳性、病情进展迅速、主动脉瓣口血流峰速>5.0 m/s,并且预期手术死亡风险低于1.0%时可选择AVR,而不符合上述情况者则建议随访观察的保守治疗。这种处理策略的考量,首先是基于观察到无症状AS死亡率低,因此手术可推迟至症状出现时;其次,许多年长患者可能在死于其他疾病之前尚不至于出现症状,甚至对于在某个时段需要手术的较年轻患者,推迟手术意味着1%~2%的患者可获得额外的生存期限;第三是鉴于人工瓣本身存在的风险,如生物瓣的退行性变、感染性心内膜炎的风险,机械瓣抗凝治疗的相关风险等。但是,这种考量忽视了患者一旦出现症状,其平均生存期仅为2~3年,猝死风险高;另外,所谓的症状可非常隐匿,为一般的病史询问所忽略。
无症状性SAS患者的管理策略
既往无症状的SAS患者一旦出现临床症状,即使仅有几个月的忽视,预后也会极差。因此,建议无症状性SAS患者一旦出现新发临床症状,应及时就诊。一些患者可能潜意识已经适应并降低自己的活动量,超过1/3的 “无症状”AS患者运动负荷试验可产生症状。但是,在运动试验中出现临床症状时要考虑以下因素:①并发的冠状动脉疾病症状与SAS症状相似;②不同患者症状的表述受个体体能状态影响,建议每位无症状性SAS患者都需接受6~12月的密切临床随访,如果在每相隔6个月的2次独立检查中,超声结果未提示疾病进展,患者应继续接受临床随访并每年行超声心动图检查。如果患者的临床状态发生变化,应尽快进行再评估。
大多数无症状SAS,最合理的治疗方案是密切随访观察。采取随访观察策略时,应当明确出现症状后应及时手术,意味着必须是在数周内而非数月内实施AVR。重视对于患者的随访和宣教工作,及时检出那些症状隐匿或由于刻意减少活动而无明显症状的患者,运动负荷试验或6分钟步行距离测试有助于临床判断。运动试验阳性或合并有1个以上高危因素者应及时行预防性手术,目前手术死亡率和并发症发生率都非常低。
SAS患者通常伴发高血压,对于无症状AS患者的高血压应积极控制。他汀类药物在延缓无症状性SAS病情进展方面的资料有限。对于合并高血压的无症状SAS患者,可能更应适时及早AVR,以保护左心室功能。
(编辑 孙煜)
[下一页] [1] [2] [3]