 陆国平 上海交通大学医学院附属瑞金医院
陆国平 上海交通大学医学院附属瑞金医院
温故1:阿托伐他汀完整的证据链
阿托伐他汀的临床研究超过400项,入选患者超过80 000例,是迄今为止获得证据最多的他汀类药物,阿托伐他汀的研究证据具有两个特征:一是完整性,二是开创性。
阿托伐他汀抗动脉粥样硬化证据链的完整性体现在以下几方面:
1.具有从降脂疗效、斑块终点到临床硬终点的完整研究证据;
2.各研究证据具有一致性结果,即强效降低胆固醇,强效稳定并逆转斑块,强效降低心血管事件风险。其中,只有降低心血管事件风险的硬终点证据才能指导临床和影响指南,而替代终点证据只有与硬终点证据相结合才能彰显其价值;
3.阿托伐他汀的硬终点证据覆盖各类人群,且覆盖10~80 mg全剂量范围,既有安慰剂对照研究,也有活性药物对照研究。这些研究一致显示了阿托伐他汀的强大获益。
阿托伐他汀研究证据的开创性对推动指南更新意义重大(图1)

(一)ASCOT-LLA和CARDS研究为特定危险人群的他汀治疗提供证据
ASCOT-LLA研究证实,对胆固醇正常或轻度升高的高血压患者,在降压治疗基础上加用阿托伐他汀10 mg/d治疗3.3年,就可进一步使冠状动脉事件风险降低36%,卒中事件风险降低27%。基于ASCOT-LLA研究,2004年发表的ATP Ⅲ补充报告,推荐中等高危患者的LDL-C治疗目标可降低至<100 mg/dl。
CARDS研究是第一个针对糖尿病患者的他汀一级预防研究,证实对于年龄>40岁、无心血管病史的2型糖尿病患者使用阿托伐他汀10 mg/d可显著降低心血管事件风险达37%。基于CARDS研究,2007 ADA糖尿病管理指南推荐年龄40岁以上的糖尿病患者无论基线LDL-C水平,均应启动他汀治疗使LDL-C降至<100 mg/dl。
(二)PROVE IT、TNT和IDEAL研究为高危和极高危患者强化他汀治疗提供证据
他汀在冠心病二级预防中的作用早经证实,针对冠心病或急性冠状动脉综合征(ACS)等高危、极高危人群,如果强化他汀治疗使LDL-C降得更低,能否更多获益? PROVE IT入选ACS患者,TNT和IDEAL研究入选稳定性冠心病患者,结果一致显示,无论ACS患者还是稳定性冠心病患者,使用阿托伐他汀80 mg/d强化治疗与常规他汀治疗相比,均能进一步降低心血管事件风险。
基于PROVE IT研究结果,2004 年发表的ATP Ⅲ补充报告,提出极高危患者可将LDL-C降至<70 mg/dl。基于TNT和IDEAL研究,2006年ACC/AHA发表更新的《冠心病二级预防指南》,指出对于所有冠心病患者,把LDL-C降至<70 mg/dl是合理的。并特别强调,对于基线胆固醇很高,不能达标的患者,LDL-C需达到50%以上的降幅。
(三)SPARCL研究为缺血性卒中患者的他汀治疗提供证据
既往卒中患者的他汀治疗依附于冠心病,SPARCL是首次专门针对卒中患者进行的他汀研究,结果证实,卒中患者使用阿托伐他汀80 mg/d治疗,可显著降低再发卒中风险达16%和各种心血管事件风险达35%。SPARCL研究使他汀成为缺血性卒中二级预防的基石。2008 欧洲卒中组织(ESO)指南和2011 ESC/EAS脂质异常防治指南均强调,所有非心源性缺血性卒中应使用他汀。
(四)ARMYDA系列研究和NAPLESⅡ研究为PCI术前的他汀治疗提供了证据
ARMYDA-1、ARMYDA-ACS、ARMYDA-RECAPTURE和NAPLES Ⅱ研究一致显示,无论稳定性冠心病患者还是ACS患者,无论择期经皮冠状动脉介入治疗(PCI)还是紧急PCI,无论之前是否使用他汀,PCI术前给予大剂量阿托伐他汀强化治疗,可显著降低围术期心肌梗死(MI)风险达44%和术后30天内主要不良心脏事件风险达44%。正是基于上述研究,2011 ACCF/AHA/SCAI经皮冠状动脉介入治疗指南强调,PCI术前给予大剂量他汀治疗以降低围术期MI是合理的(Ⅱa,A/B)。
温故2:阿托伐他汀的强大心血管获益
阿托伐他汀的强大心血管获益不只体现在上述研究中心血管事件风险的大幅度降低上,还体现在开始出现获益的时间更快(图2)。Ray 和 Cannon教授曾联合撰文认为:获益时间正成为临床选用他汀的重要评估指标。获益更早的药物,使患者更早脱离高风险状态。多项研究显示,阿托伐他汀在多种人群均显示更早获益。在高血压和糖尿病患者,阿托伐他汀开始出现获益的时间为1~4个月,其他他汀需1~1.5年;在冠心病和ACS患者,阿托伐他汀开始出现获益的时间为1个月,而其他他汀需4~6个月。另外,多项PCI围术期研究显示,术前使用阿托伐他汀强化治疗更可将获益提前至围术期。

知新:阿托伐他汀强大心血管获益机制何在?
阿托伐他汀强大心血管获益的机制源于其独特的分子结构(图3)。他汀类药物化学结构的相同点在于:均有对HMG-CoA还原酶有抑制作用的药效基团(二羟基庚酸基团)。他汀类药物化学结构的不同点在于:与药效基团相连的取代基不同,这决定了他汀类药物药代学和临床疗效及安全性的差异。
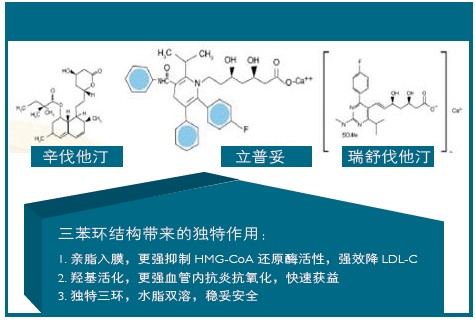
阿托伐他汀化学结构中的取代基是由共价连接到三个芳香结构(苯环)的吡咯环组成。这种三环结构是阿托伐他汀独有。三环结构独特之处有三:
1. 亲脂入膜,快速强效。立普妥的三环结构有助于增加其脂溶性,有利于进入各种靶细胞膜,快速发挥强效抑制HMG-CoA还原酶活性,同时可通过影响膜离子转运或信号转导快速发挥多效性作用。
2. 羟基活化,更强抗炎抗氧化。三环结构在CYP450酶的作用下,可羟基活化,生成邻/对位羟基代谢产物。这些代谢产物类似于多酚样物质,具有还原作用,同时在细胞膜可通过质子捐赠和共振稳定机制灭活氧自由基,发挥抗氧化作用,这一作用阿托伐他汀母体和其他他汀无法复制。另外,这些代谢产物可直接进入血液循环,与阿托伐他汀母化合物在血管壁共同发挥强大的抗炎抗氧化作用。辛伐他汀经肝脏代谢后95%经肝脏吸收,不到5%的活性成分进入血液,无法发挥血管内的抗炎抗氧化作用。瑞舒伐他汀以原形进入血液循环,原形抗氧化作用弱,代谢产物活性低或无活性。
3. 水脂双溶,稳妥安全。由于羟基的存在,增加了其亲水性,这是一个与脂溶性完全相反的效果,使阿托伐他汀水脂双溶,减少了脂溶性他汀细胞膜相关的安全性问题。这或许可解释同为脂溶性他汀,辛伐他汀和西立伐他汀存在严重肌肉安全性风险,而阿托伐他汀则具有良好的肌肉安全性,同时阿托伐他汀不经肾脏代谢使其拥有更好的肾脏安全性。
小结
与其他他汀相比,阿托伐他汀积累了完整的证据链,对推动他汀抗动脉粥样硬化治疗贡献卓越。阿托伐他汀在抗动脉粥样硬化治疗中显示了强大的心血管获益:即可大幅降低心血管事件风险,又可更早带来事件的降低。阿托伐他汀的完美证据链和强大获益源于其独特的分子结构带来的更强降LDL-C作用和更多降脂外作用。
[下一页] [1] [2]