 2010年心房颤动(房颤)领域一大批新的研究成果陆续公布,为临床诊疗提供了新的思路和佐证。盘点2010年,各项研究精彩纷呈,房颤消融的有效性得到进一步验证,房颤抗凝治疗进一步细化,新的抗凝药物和血栓栓塞风险评估系统得到验证,欧洲心脏病学会(ESC)发布了新的房颤治疗指南[1],以及美国心脏病学会基金会/心脏病协会/心律学会(ACCF/AHA/HRS)网上发布了房颤指南更新[2],为房颤诊治提供了更加科学的依据。
2010年心房颤动(房颤)领域一大批新的研究成果陆续公布,为临床诊疗提供了新的思路和佐证。盘点2010年,各项研究精彩纷呈,房颤消融的有效性得到进一步验证,房颤抗凝治疗进一步细化,新的抗凝药物和血栓栓塞风险评估系统得到验证,欧洲心脏病学会(ESC)发布了新的房颤治疗指南[1],以及美国心脏病学会基金会/心脏病协会/心律学会(ACCF/AHA/HRS)网上发布了房颤指南更新[2],为房颤诊治提供了更加科学的依据。
房颤机制新认识
基于近年来临床和基础的大量研究,ESC发布的新的房颤治疗指南细化了房颤机制:心房因素(心房病理生理学改变,如心房扩大或纤维化等),电生理机制(局灶激动或折返,多个微折返等),遗传因素(如心肌钠离子通道基因SCN5A调节功能缺失等),临床相关因素(如血流动力学改变等) [1]。
新危险因素:肥胖和OSAS
肥胖 房颤患者的平均体重指数(BMI)为27.5 kg/m2,相当于当于中等肥胖[3]。超重和肥胖能影响心房和心室结构、心室舒张功能、自主神经功能,提示肥胖与房颤有明确关联。资料表明,肥胖者的房颤相对风险是正常个体的1.5倍,且BMI每增加1 kg/m2,房颤的相对风险上升4%[4]。
睡眠呼吸障碍 睡眠呼吸暂停综合征(OSAS)因增加心房压或自主神经张力的过度变化能促发房颤。反复血液动力学和低氧起伏波动还能激活牵张敏感性离子通道和(或)儿茶酚胺敏感性通道,导致更活跃的局灶激动。OSAS伴发的迷走反射(以心动过缓为标志)可导致肺静脉前庭的不应期缩短,促发局灶性激动。此外,OSAS还与C反应蛋白升高独立相关,导致房颤的相对风险增加。研究表明,房颤患者OSAS的患病率明显高于无房颤组(49% vs. 32%,P<0.001)[5]。
房颤分型
ESC发布的房颤治疗新指南将房颤分为五类:首次诊断的房颤、阵发性房颤、持续性房颤、长程持续性(long-standing persistent)房颤、永久性房颤。增加了长程持续性房颤的概念,定义为房颤持续时间超过1年,拟采用节律控制策略,即包括导管消融治疗[1]。这一概念是适应了目前的导管消融治疗新时代的特殊名词,无庸置疑,导管消融使房颤治愈成为可能,可以遏制逆转房颤致房颤的的重构进程,房颤不再是永久性。
治疗目标
ESC发布的房颤治疗新指南新指南首次把“住院”与“死亡,卒中”一起列入前三位的房颤治疗目标[1]。提高了房颤治疗终点事件的地位,强调抗心律失常药物治疗的安全性,加强患者随访,重视患者的再住院率,积极减少心血管事件的发生率。房颤治疗目的旨在缓解症状、减少住院,减少心血管事件、提高生存率。
抗凝
近一年多个大规模临床试验为房颤抗凝领域带来了新的证据。2010年ESC年会上公布的新指南强调抗凝治疗是预防房颤患者卒中发生的最佳手段。根据欧洲房颤调查研究[6],增加和调整了卒中与血栓栓塞的危险因素,建立了新血栓风险评估系统: CHA2DS2-VASc评分,确定了基于 CHA2DS2-VASc评分系统的抗凝策略,将危险因素分为主要危险因素(包括既往卒中,短暂性脑缺血发作或全身性栓塞)和临床相关的非主要危险因素[包括心力衰竭、中重度左室收缩功能不全(如LVEF≤40%)、高血压、糖尿病、女性、血管疾病、年龄65~74岁],其在CHADS2积分基础上将年龄>75岁由1分增加为2分,新增血管疾病、年龄65~74岁、性别(女性)三个危险因素。新指南关于选择口服抗凝药物的建议:抗栓治疗的选择应基于卒中、血栓栓塞和出血的绝对风险以及风险获益比(ⅠA)。除了低危患者(孤立性房颤、年龄<65岁)或存在禁忌征,所有房颤患者均应行抗栓治疗以预防血栓栓塞并发症(Ⅰ,A)。评分≥2分,口服抗凝药物(Ⅰ,A);评分1分,口服抗凝药物(Ⅰ,A)或阿司匹林75~325 mg(Ⅰ,B),优先推荐口服抗凝药物(Ⅱa,B);评分0分,口服阿司匹林或不应用任何抗栓药物,优先推荐不应用任何抗栓药物。新指南仍推荐控制INR 2~3。
ESC发布的房颤治疗新指南房颤预防血栓栓塞策略特点:
1.细分了CHADS2分级中的0~1分人群抗凝策略;
2.大大增加了“高危”和“高分”人群,如女性1分,>65岁的高血压=2分,65岁以上的女性高血压CHA2DS2-VASc评分3分;
3.阿司匹林地位下降,进一步提升了口服抗凝药物的地位;
4.抗凝表现为“全或无”,即应用或不应用口服抗凝药物。
欧洲心脏调查研究根据HAS-BLED评分[高血压、肝/肾功能异常、中风、出血史或出血倾向、INR不稳定、老年(年龄>65岁)、药物/酒精成瘾,各1分]评估房颤患者抗凝出血风险[7]。结合2010年发布的急性冠脉综合征或冠脉介入房颤患者抗栓治疗共识[8],新的指南强调房颤患者应用抗栓药物(阿司匹林或氯吡格雷)应警惕出血,特别是冠脉支架植入术后,具体如下表。
房颤血栓栓塞高危(需要口服抗凝药物)患者冠脉支架植入术后抗凝策略
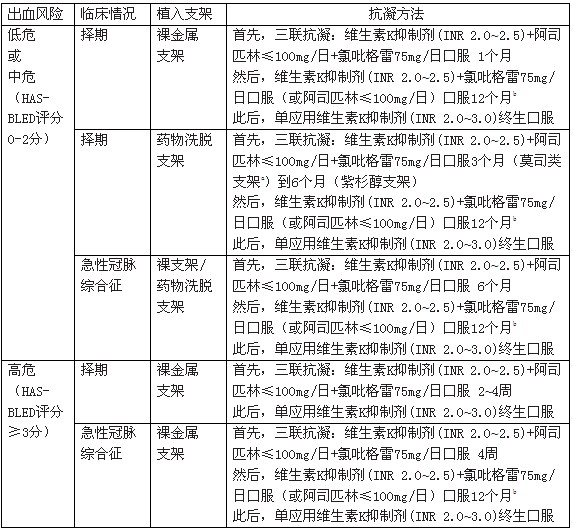
INR:国际标准化比值
必要时应给予质子泵抑制剂保护胃粘膜
a:西罗莫司,依维莫司,他克莫司
b:联合使用维生素K抑制剂(INR 2.0~2.5)+氯吡格雷75mg/日口服(或阿司匹林≤100mg/日)口服12个月
c:药物洗脱支架应尽可能避免,但如果植入药物洗脱支架,必要时应考虑延长三联抗凝时间(3~6个月)。
根据Lip等修订
对于不适合应用华法令的房颤患者,ACTIVE研究[9]显示联合阿司匹林和氯吡格雷口服可有效降低卒中。因此美国ACCF/AHA/HRS更新的房颤治疗指南推荐对于当由于患者不愿接受华法令治疗或医生出于安全考虑不建议应用华法令,联合阿司匹林和氯吡格雷口服预防主要血管事件,包括中风(Ⅱb,B)。
ROCKET-AF研究[10]是一项房颤抗凝的随机双盲对照研究,入选45个国家1100个中心共计14 000多名心房颤动患者, 随机分配凝血Xa因子抑制剂利伐沙班组(口服20mg/日,若有中度肾功能不全则为15mg)或华法林组(口服华法令,调整剂量置INR达2.5)。比较利伐他班和华法林对非瓣膜性房颤中风的预防作用。该研究将被试验患者风险较高,55%有中风病史,90%有高血压。此外,90%的患者CHADS2得分3分或者更高。结果显示在各种原因所致的中风和非中枢神经系统(CNS)栓塞方面,口服利伐沙班不劣于华法林。在出血方面,应用新的抗凝治疗的患者中出现致命性的出血和颅内出血相对较少。值得注意的是,该研究入选患者平均年龄73岁,卒中风险较高,55%有中风病史,90%有高血压。此外,90%的患者CHADS2得分3分或者更高。因此,该研究作为一项非劣性研究,结果显示利伐沙班可有效、安全替代华法令抗凝。为未来房颤抗凝提供了更多选择,前景广阔。
由于美国FDA尚未批准Watchman器械封堵左心耳预防血栓栓塞,因此,这一方法在指南更新中未推荐使用[2]。
药物控律与控率
常用的抗心律失常药物(AAD)包括胺碘酮、决奈达隆、氟卡尼、普罗帕酮和索他洛尔(均为Ⅰ,A)。迄今为止,胺碘酮仍然是所有AAD中维持窦性心律疗效最好的药物(Ⅰ,A)。DIONYSOS研究[11]显示决奈达龙尽管转律疗效逊于胺碘酮,但毒副作用明显少于胺碘酮,验证了其安全性。ESC公布的新指南强调了决奈达龙的药物治疗地位,可有效用于于合并冠心病、高血压性心脏病或稳定性心衰(心功能I或II级)的房颤患者,特别是对于稳定性心衰患者,决奈达龙可显著降低住院率。ATHENA研究[12]显示决奈达龙(400mg,2次/日)可有效降低死亡率和心血管住院联合终点,在美国ACCF/AHA/HRS在房颤指南更新中,决奈达龙地位进一步提升,推荐应用决奈达龙用于房颤转律,并降低阵发性房颤和持续性房颤转律后心血管住院率,可作为门诊房颤患者初选治疗(Ⅱa,B);决奈达龙禁止用于合并Ⅳ级心衰的房颤患者或近4周出现失代偿心衰,特别是左室功能显著降低的房颤患者(Ⅲ,B)。对于不合并器质性改变或冠心病的门诊阵发性房颤患者,推荐窦律时首选普罗帕酮或氟卡尼(Ⅱa,B)。
ESC新的抗房颤药物维纳卡兰(Vernakalant)用于临床,其静脉应用90min内的房颤转复率显著高于胺碘酮(51.7% vs. 5.7%),显示了良好的前景[13]。
最近在新英格兰杂志发表的RACE Ⅱ研究[14]显示永久性房颤患者宽松的心率控制和严格的心率控制无论在临床症状,还是副作用方面,二者相似。因此ESC新的指南建议,采用宽松的心率控制策略,药物选择包括β受体阻滞剂、非二氢吡啶类钙拮抗剂和地高辛等。美国ACCF/AHA/HRS更新的房颤治疗指南也建议:尽管长期心动过速可导致可逆的心功能下降,但对于心功能稳定(LVEF>0.4)且无心律失常相关症状的持续性房颤患者,严格心率控制(静息心率<80次/分或6分钟步行试验心率<110次/分)并不优于宽松的心率控制(静息心率<110次/分)(Ⅲ)。
此外,新近发表的临床研究和荟萃分析显示ACEI、ARB、醛固酮拮抗剂、他汀、ω-3多不饱和脂肪酸可作为房颤的一级和二级预防[15-17],明确了“上游治疗”在房颤治疗中的作用和地位。
[下一页] 1 [2]