 GWAS:高血压研究之未来
GWAS:高血压研究之未来
Dr. Anna F Dominiczak, University of Glasgow, U.K.
流行病学资料显示,高血压发病与遗传和环境因素联合作用有关,其中遗传性因素占30 ~ 50%。GWAS 医学基因研究史上的分水岭,数据可靠且具有可重复性。2007年首个高血压GWAS研究Wellcome Trust Case Control Consortium (WTCCC)问世后,8个血压相关GWAS相继发表,研究对象来自欧洲、日本、韩国和美国等多个国家和地区。其中CHARGE BP和 Global BP Gen的结果令人振奋。这2项研究各纳入大约3万例的研究对象,共发现了十多个阳性SNP位点(达到基因组水平上的显著意义,即P< 5x10-8),而且这些位点在大样本量的人群研究中得到验证(图1)。携带这些基因患者的血压升高具有统计学意义,其心脑血管病风险也显著增加。
在此前十多年中,采用家系连锁分析或侯选基因关联研究的高血压基因研究未获成功,GWAS终于取得了突破性进展。这些位点所在的基因或位点附近的基因,除个别外,以前均未被列为血压或高血压的侯选基因。对这些基因的深入研究,有可能揭示血压调节或高血压发生的新机制,对高血压的预防和治疗具有重要临床意义
 高血压GWAS,或已无路可走
高血压GWAS,或已无路可走
Dr. Theodore Kurtz, University of California, U.S.
当前,GWAS尽管花费了数百万美元,其结果对高血压理论和实践的指导意义甚小。GWAS还不能清楚的描绘高血压相关基因构成、揭示新的发病机制和识别出任何有价值的高血压治疗新靶点。
对高血压有微弱影响的SNP位点只能解释小于0.07 ~ 0.2%的血压改变,我们没有理由继续寻找此类基因。除了环境因素具有重要作用外,影响多因素疾病如高血压等发病的遗传因素可能很复杂,导致血压升高或降低的基因变异数量可能很多,可能有成千上万,而且不同个体、不同家庭之间,也可能千差万别,因此,靠这种大海捞针式的研究方法获得成功的可能性不大。而在长时期的生理学、病理生理学以及药理学等研究中,我们已经对许多临床特征如血压等的调节机制有了比较深入的了解,并根据这些知识,研究并发展了大量有效的治疗药物,可以有效控制高血压等复杂疾病,预防各种严重致死、致残性并发症。目前没有证据显示,GWAS发现的候选治疗靶点优于通过其他方法发现的治疗方法。CHARGE协议中,危险评分根据GWAS研究中发现的前10个基因位点对收缩压的联合作用进行,但是基因风险评分并非是一个有用的工具(图2)。我认为,即使所有高血压相关的基因位点能够被识别,其对于临床高血压诊治的指导意义不会优于目前的临床危险分层。
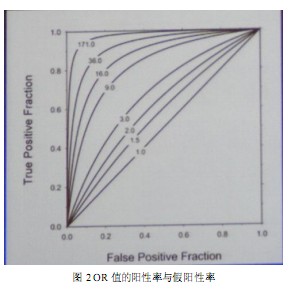
随着技术提升、成本降低,利用SNP高通量检测手段,对人类全基因组进行“地毯式”排查,为全面系统研究复杂疾病的遗传因素掀开了新的一页,是目前科学界公认的最为有效的搜寻重大疾病易感基因的研究方法,但是在高血压临床研究应用方面仍需探索新的途径和方向。
 GWAS揭示的仅是冰山一角
GWAS揭示的仅是冰山一角
朱鼎良 上海市高血压研究所
2007-2009年发表的与血压或高血压有关的GWAS论文有12篇, GWAS发现的基因变异对血压的影响很小,单个风险等位基因使收缩压平均升高1mmHg,使舒张压升高0.5mmHg。血压或高血压病的遗传度在30~50%左右,但这十多个位点的共同作用只能解释人群中约1%的血压差异。因而,GWAS只是揭开了血压和高血压相关基因的冰山一角,更多的相关基因有待识别。
对于身高、体重指数等性状,GWAS存在同样问题。如身高的遗传度高达90%,但GWAS发现的20个相关位点的共同作用只能解释人群中约3%的身高差异。为何GWAS只能揭开基因全貌的冰山一角?常见变异-常见疾病(common variant/common disease)假说认为,常见的复杂性状疾病涉及多个常见基因变异,其中每个基因变异对疾病性状的影响微弱。GWAS采用的芯片只能检测频率较高(MAF>5%)的常见基因变异,不能检测低频的基因变异。因此GWAS研究结果表明,常见变异-常见疾病假说不完全适用于常见复杂性状疾病。低频的少见变异(rare variant)对性状的作用可能大于常见变异的作用,多个少见变异共同作用同样可导致常见疾病。检测少见变异需要采用新一代的测序技术,通过基因重排序(resequencing)发现低频的基因变异。
高血压基因研究的今后走向可能有:(1)建立国际性或地区性协作组,对GWAS研究结果进行meta分析。扩大样本量可以提高GWAS的统计功效, 可能发掘出一些频率相对较低的常见变异;(2)目前高血压GWAS主要集中在欧美白人,需要黑人和亚洲人群的资料;(3)对GWAS已发现的相关基因变异开展功能研究;(4)开展少见变异的关联研究。
 多因素疾病病因研究的思考
多因素疾病病因研究的思考
王继光 上海交通大学医学院附属瑞金医院
GWAS作为一种较新的遗传学研究方法已经有十余年的历史了,主要用于有遗传倾向的多因素疾病的病因学研究。由于基因分型能力有限,早期的此类研究多选择基因组中数百或上千个微卫星标记,根据财力大小,对数百甚至数千名所谓的“病例”和“正常对照”进行分型,寻找可能与疾病有关的染色体片段。尽管非常昂贵,这类研究还是进行了很多,仅在血压研究领域,全球范围内,公开发表的独立研究报告就有30多项,可能还有很多从未公开发表。多数研究都有一些位点达到了统计学显著水平,但遗憾的是,并未能在此基础上进一步找到任何与血压调节或高血压发病有关的基因或基因变异。
近年来,随着基因分型能力和计算分析能力的大幅度提高,在进行此类研究时,已改为选择数万、数百万或更多SNP变异位点,对数百、数千、甚至数万“病例”和“正常对照”进行分型,寻找可能与疾病有关的基因变异位点。截至目前,在血压领域,已经有十余项研究报告发表。结果和微卫星标记时期的此类研究十分相似,也发现了一些统计学显著的位点,但同样遗憾的是,这些位点所影响的血压大多不到1 mm Hg,所解释的血压变异也在1个百分点以下。因此,可以预期,这些研究对阐明多因素疾病的病因与发病学不会有太大帮助。
遗传学研究不能撇开历史,相反应利用先进的基因组学方法在病理生理学的基础上进行深入研究,并进一步丰富病理生理学的内涵。比如,使用传统的病例生理性手段,许多蛋白质如受体的研究工作十分困难,但使用基因标记则有许多优势,基因高度稳定,通常一生不变;基因分型简易而准确;基因变异所带来的功能差异往往是长期的。
建立在基因结构变异基础上的遗传学研究方兴未艾。也许在技术本身不再“fashionable”时,我们才会不再热衷于“高技术、大工程”,而更多思考问题,讨论问题,多因素疾病的病因学研究也才能大放异彩。对高血压等多因素疾病而言,关键是要首先要建立准确的表型,特别是前瞻性变化的表型。
 高血压GWAS的困惑与希望
高血压GWAS的困惑与希望
牟建军 刘富强 西安交通大学医学院第一附属医院
GWAS是从人类全基因组范围内的序列变异中筛选出与疾病性状关联的SNP。其优势在于,不再受预先设定的候选基因限制,使得众多功能不明的基因及大量基因间区域的SNP都为疾病的研究提供了线索。然而近年在新英格兰杂志发表了数篇文章辩论GWAS研究的是否有现实意义。因为总结历年的GWAS病理/对照研究数据,发现花费数亿美元的GWAS研究,最后获得的大部分biomarker,对疾病预测的贡献值都非常小,低于7%,而且多数实验结果无法被别人所重复。因此有学者开始对GWAS研究复杂疾病的策略和思路提出了质疑。
高血压是遗传与环境因素相互作用的疾病。原发性高血压研究的一项主要任务是阐明血压升高的遗传学机制,也就是寻找高血压相关基因。虽然多数单基因遗传性高血压疾病的致病基因及其致病突变已被阐明,但发现新病种、新致病基因和新的致病突变还有不少工作可做。目前已列出的高血压侯选基因数目不下200种,它们分别与以下系统或功能有关:肾素-血管紧张素-醛固酮系统、交感神经系统、下丘脑-垂体轴、内皮素、利钠肽、激肽释放酶-激肽系统、类固醇激素、前列腺素、生长因子和激素、骨架蛋白和粘附分子、细胞内信使。脂质代谢、糖代谢、载脂蛋白、离子通道或转运体等,但迄今突破点不多。目前已有应用GWAS技术对其进行大规模的研究,如Framingham Heart Study和Wellcome Trust Case Control Consortium,但他们的结果也不尽相同。这需要我们进一步思考其深层次原因。高血压是多基因网络和多种环境因素相互交织反应
[下一页] [1] [2] [3]