高盐促进高血压、心血管及肾病的发生
盐摄入过多已被证实是引发高血压的一个重要环境因素。目前世界范围内的许多盐与高血压的关系资料均表明,盐的摄入量与血压升高呈正相关。INTERSALT研究发现,每日钠盐摄入量增加5~6 g,其收缩压水平增高3.1~6.0 mmHg,舒张压增高0.1~2.5 mmHg,首次在较大样本量、多人群中证实了钠盐摄入量是决定血压水平的最重要因素。需要强调的是,不同个体对盐负荷或减少盐的摄入呈现不同的血压反应,即存在所谓盐敏感性问题。血压的盐敏感性是指相对高盐摄入所引起的血压升高,与人体钠泵基因突变有一定的关联。在我国,一般人群中盐敏感者占15%~42%,原发性高血压群体中盐敏感者可达60%左右。研究发现伴有慢性肾病、肥胖、高龄、代谢综合征、糖尿病和非裔美国人的高血压患者对盐的敏感性较高。
近年来关于盐与心血管疾病之间的关系引起人们的关注。芬兰的研究显示, 无论男性还是女性,与24h尿钠排泄上升100 mmol有关的冠心病、心血管疾病和总体死亡率的风险比率分别是1.51、1.45和1.26。另一项荟萃分析结果显示高盐饮食显著增加心血管事件总体风险17%。以上研究提示血压的盐敏感性是心血管发病的一个独立危险因子。
盐对于肾脏疾病也有着重要的影响。高盐饮食可减少肾血流量,并增加肾小球滤过率。研究显示,在摄入钠(200 mmol/d)1周后,有微量白蛋白尿和显性白蛋白尿的患者的钠敏感指数(压力-尿钠排出曲线斜率的倒数)中位数和平均血压均高于无白蛋白尿的正常人群。
此外,钾摄入量过低或钾 / 钠比值降低也可导致心血管疾病、高血压的发生。INTERSALT研究提示,钾的排泄量与收缩压、舒张压均呈稳定、独立的负相关关系;因此,对临床医生而言,钾摄入量和钾 / 钠比值的重要性也不应忽视。
高盐导致心血管疾病发生的机制
高盐促进心血管疾病进展的机制目前尚未完全阐明,一般认为可分为血压依赖性和非血压依赖性。血压依赖性即高盐可通过水钠潴留、细胞水肿、增加血管对儿茶酚胺的敏感性、抑制钠-钙交换、使细胞钙排出减少等直接导致血压升高,引起心血管疾病和肾功能不全的发生。
非血压依赖机制包括:血管内皮细胞对局部血管张力和血流动力学起重要的调节作用。Claudio等研究发现与盐抵抗者相比,盐敏感者高盐饮食后血浆内皮素-1水平显著升高,尿白蛋白排泄显著增加。因此,内皮功能损伤可能是盐敏感性高血压靶器官损伤和心血管危险的重要病理机制。此外,持续的高氧化应激水平也可引起心血管疾病和肾功能不全的发生。
RAS(肾素-血管紧张素)系统是在心血管疾病发展中起重要作用的激素系统。研究表明,盐摄入与AngII在多个方面相互影响,其作用机制可能与细胞水平有关。BAYORH等将12只Dahl盐敏感大鼠分为两组,分别接受正常盐量(0.3%NaCl)或高盐量(8%NaCl)饮食三周后发现,高盐摄入的大鼠其血浆RAS活性下降,但心脏和肾脏的AngII却显著增加。另一项动物研究发现,给予盐敏感大鼠连续5周高盐饮食后,组织(心室、近曲小管)ACE浓度明显增高,心脏和血管纤维化程度加剧。此外,由于低盐饮食常常导致患者RAS系统过度激活的可能危害,而抵消了低盐饮食降低血压所带来的心血管获益。
高盐高血压患者的治疗
减少钠盐摄入是高盐高血压患者的一项重要血压控制措施。《中国高血压防治指南2005》推荐北方首先将每人每日平均食盐量降至8 g,以后再降至6 g;南方可控制在6 g (尿钠排泄量为100 mmol/d)以下。但对于多数中国患者而言,限盐的可行性差。一方面是由中国饮食特点决定的;另一方面即使限盐患者也可能转向诸如酱油这样其他的含盐的调味品。此外,INTERSALT等研究表明限盐策略(食盐量控制在6 g/d)仅能降低高血压患者血压4~6/2~3 mmHg,且限盐策略对高血压患者心血管硬终点减少的证据尚有争议。因此,药物治疗对于大多数高血压患者的降压达标和降低心血管事件仍是必须的。
一般认为,高盐高血压患者降压药物应首选钙离子拮抗剂(CCB)和利尿剂,尤其是调节型盐敏感高血压患者。利尿剂通过利钠缩容而降低血压,且价廉物美,更适合中国国情。有研究报告,盐敏感性高血压患者经氢氯噻嗪25 mg/d治疗6周后,收缩压及舒张压均明显降低,其中收缩压平均降低52 mmHg,舒张压平均降低18 mmHg,尤以中青年中度的盐敏感高血压降低最为显著。但长期以来对糖脂代谢的不良影响的担忧,使得利尿剂的临床使用很局限。事实上,在对12 550例45~64岁无糖尿病的患者为期6年的调查结果提示,校正各种混淆因素后,与安慰剂相比,小剂量利尿剂并不会导致患者新发糖尿病的风险增加,说明小剂量利尿剂长期使用是安全的。因此目前临床上推荐使用小剂量利尿剂,如氢氯噻嗪12.5 mg/d。
由于剂量的限制,利尿剂的降压效果也受到了限制。联合降压药物治疗是高盐高血压患者必然的优效选择。 在Steven G 等人的研究中,397例盐敏感性高血压患者在给予高盐或低盐饮食下随机接受ACEI和CCB治疗,结果显示高盐饮食情况下ACEI和CCB的降压疗效一致;而在低盐饮食期间,ACEI的降压疗效更为优越,(11.3 / 7.7 mmHg vs. 7.7 /4.8 mmHg,P<0.02)。国内外研究也发现,组织亲和力高的ACEI贝那普利同样也可有效降低盐敏感高血压患者的血压,尤其是非调节型盐敏感高血压患者。
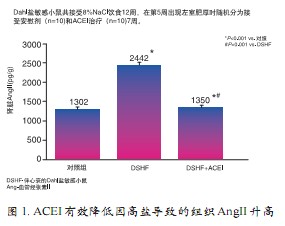
其次,高盐环境下存在非血压依赖的靶器官损伤,因此对高盐高血压患者的心脑肾疾病的预防更为重要. 研究显示高盐导致的组织RAS的激活可以被ACEI抑制。动物研究显示,高盐饮食的Dahl盐敏感小鼠接受ACEI治疗7周后,ACEI组肾脏的AngII较安慰剂组均明显降低(图1),提示ACEI可有效减少因高盐导致的组织AngII升高。
2009年欧洲高血压指南再评价及2010年美国高血压学会联合治疗的推荐中,利尿剂和ACEI的联合是降压治疗的优选方案之一。ACEI与利尿剂之间存在协同降压作用。ACCOMPLISH研究中,贝那普利/氢氯噻嗪组血压控制率高达72.4%,高于目前其他大型临床研究的血压控制率。并且贝那普利/氢氯噻嗪治疗52周后显著降低高危高血压患者左室质量指数。
综上所述,ACEI拥有全面靶器官保护,是欧美指南高血压患者适应证推荐最多的药物。对于高盐高血压患者,ACEI与利尿剂的联合治疗兼顾降压与靶器官保护,是临床的理想选择。
结语
饮食中的高盐摄入不仅与血压关系密切,还通过氧化应激,内皮功能异常和组织RAS激活导致靶器官损伤从多个方面加速心血管疾病的进展。对于高盐高血压患者,在饮食上要科学合理的限盐补钾,食盐量控制在6 g/d。此外,ACEI/氢氯噻嗪联合在强力降压的基础上提供全面靶器官保护,是此类患者的优选治疗方案之一。